新冠肺炎可以牵一发而动全身
已知的七种人类冠状病毒家族以其对呼吸道的影响而闻名,而不是对心脏的影响。然而,最新的冠状病毒,严重急性呼吸综合征冠状病毒2(SARS-CoV-2),具有明显的心脏趋向性,可导致心肌炎(心脏炎症)、细胞坏死、模仿心脏病发作、心律失常以及急性或长期心力衰竭(肌肉功能障碍)。这些并发症有时是冠状病毒病2019年(新冠肺炎)临床表现的唯一特征,即使在症状轻微的病例和没有任何症状的人中也会发生。最近关于年轻运动员涉及心脏的发现,包括猝死,引起了人们对我们目前知识的限制以及新冠肺炎心脏表现的潜在高风险和隐匿性流行的担忧。
四种“普通感冒”人类冠状病毒-HCoV-229E、HCoV-NL63、HCoV-OC43和HCoV-HKU1-与心脏异常无关。中东呼吸综合征(MERS;由中东呼吸综合征冠状病毒(MERS-CoV)引起)合并心肌炎的患者和少数SARS患者(由SARS-CoV引起)心脏病的病例系列有孤立的报道(1)。因此,SARS-CoV-2的一个明显特征是其更广泛的心脏受累,这也可能是大流行和数千万人接触该病毒的后果。
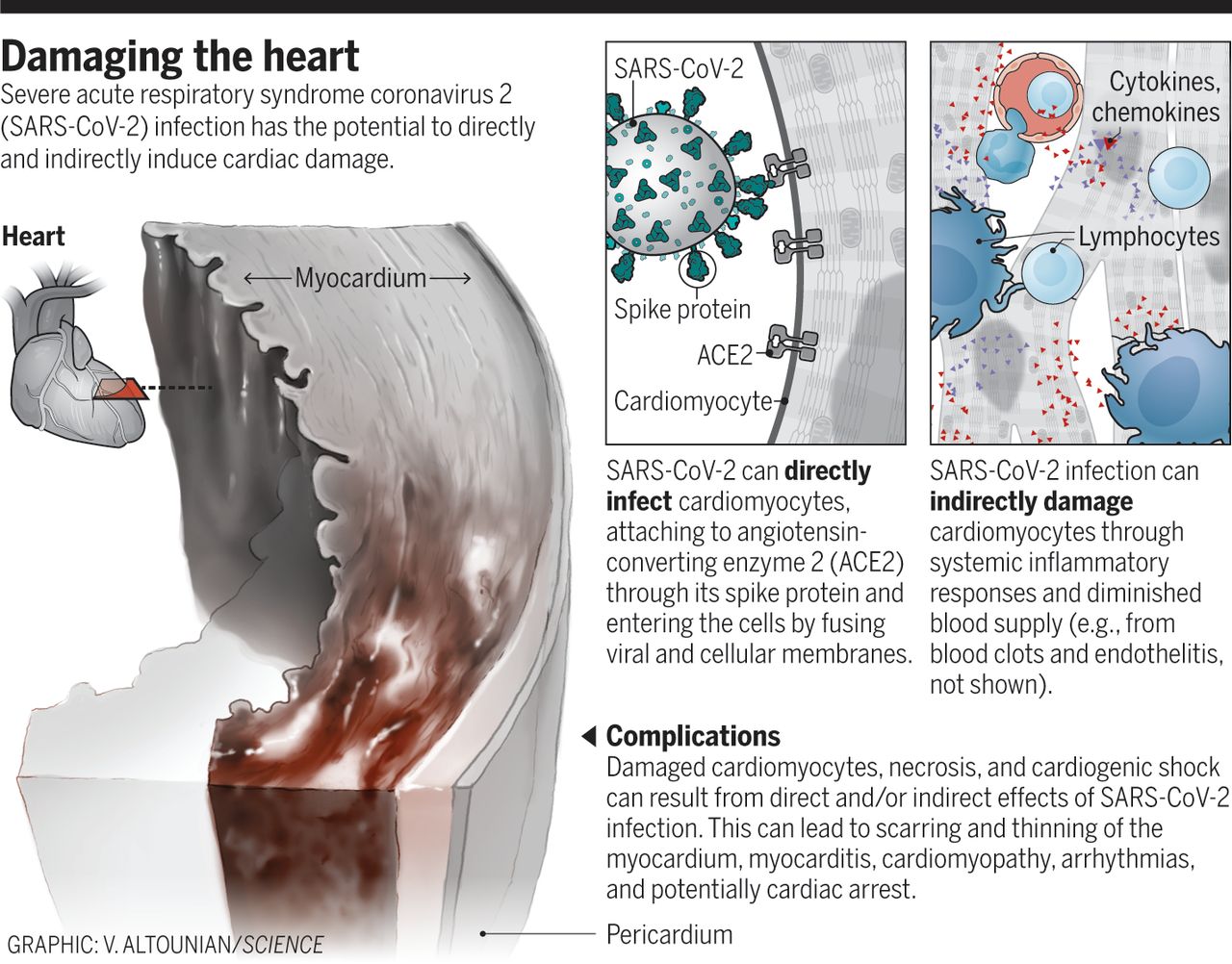
在结构上将SARS-CoV-2与SARS区分开来的似乎是一个呋喃多碱位点,当它被切割时,可以扩大病毒可以感染的细胞类型(嗜性)[2]。该病毒以全身血管紧张素转换酶2(ACE2)受体为靶标,通过其刺突蛋白以及细胞丝氨酸蛋白酶跨膜蛋白酶丝氨酸2(TMPRSS2)、硫酸乙酰肝素和其他蛋白酶的协同作用促进细胞进入(3)。心脏是ACE2高表达的众多器官之一。此外,SARS-CoV-2对ACE2的亲和力明显大于SARS(4)。已经从尸检标本中研究了SARS-CoV-2对肺以外其他器官的嗜性:SARS-CoV-2基因组RNA在肺部最高,但心脏、肾脏和肝脏也显示出大量的病毒,在22名死亡患者中有16人的心脏中检测到了病毒的拷贝(5)。在新冠肺炎死亡的39名患者的尸检系列中,38%的患者在心肌中检测不到病毒,而31%的患者心脏中的病毒载量超过1,000个拷贝(6)。
因此,SARS-CoV-2感染可以直接和间接损害心脏(见图)。SARS-CoV-2在体外感染诱导多能干细胞(IPSCs)来源的心肌细胞的能力很强,导致心肌细胞碎裂的独特模式,“收缩机制完全溶解”(7)。(2)SARS-CoV-2病毒在体外可感染诱导多能干细胞(IPSCs)来源的心肌细胞,导致心肌细胞碎裂,“收缩机制完全溶解”(7)。其中一些发现是从病人尸检样本中证实的。在另一项IPSC研究中,SARS-CoV-2感染导致细胞凋亡,并在暴露后72小时内停止跳动(8)。除了直接感染心肌细胞外,病毒进入心脏和多个血管床的血管内皮细胞中也有记录。对感染的心脏和内皮细胞(内皮炎)的二次免疫反应只是许多潜在间接影响的一个方面。这些包括调节血压的肾素-血管紧张素-醛固酮系统的失调,以及涉及血小板、中性粒细胞、巨噬细胞和淋巴细胞的促炎反应的激活,细胞因子的释放和血栓前状态。在多个尸检系列和年轻的新冠肺炎中风患者中,已经报道了在微血管和大血管中都有凝血倾向。
心血管表现多种多样,从有限的心脏细胞坏死(导致损伤),到心肌炎,再到心源性休克(通常是致命的无法泵入足够的血液)。心脏损伤,由血液中肌钙蛋白(一种心肌特异性酶)的浓度反映出来,在新冠肺炎身上很常见,至少五分之一的住院患者和一半以上的既往心脏病患者都会发生心脏损伤。这种心肌损伤是住院死亡率的危险因素,肌钙蛋白浓度与死亡风险相关。此外,肌钙蛋白含量较高的患者有炎症[包括C反应蛋白、白细胞介素-6(IL-6)、铁蛋白、乳酸脱氢酶(LDH)和中性粒细胞计数增加]和心脏功能障碍(氨基端B型利钠肽原)的标志(9)。
比有限损伤模式更令人担忧的是心肌炎:心脏的弥漫性炎症,通常表现为损伤和对损伤的炎症反应的不同混合物,这种反应可以延伸到人类心脏的三层。
最近一系列接受心脏磁共振成像或超声心动图检查的新冠肺炎患者提供了一些关于心脏受累的新见解(12-14)。在新冠肺炎康复的百名患者中,78人有心脏异常,包括18名没有任何症状的患者中的12人,60人有持续的心肌炎,这与心肌炎是一致的(12人)。在与新冠肺炎一起的大型前瞻性队列中,1200多名患者中的大多数都有超声心动图异常(13)。这引起了人们对是否比预期的更普遍的心脏受累的担忧,特别是因为至少30%到40%的SARS-CoV-2感染发生在没有症状的情况下。这些人可能有潜在的心脏病理。
到目前为止,已经有四个小系列的真正感染的无症状个体接受了胸部计算机断层扫描(CT),以确定是否存在与新冠肺炎一致的肺部异常。事实上,一半无症状的人表现出与有症状的患者相同的肺部CT特征。但到目前为止,在SARS-CoV-2检测呈阳性或血清阳性但没有症状的人中进行的心脏影像学研究很少。此外,SARS-CoV-2感染后任何器官异常消退或持续的时间进程尚未报道。尽管同时有内脏损伤的证据,但静默感染的比例很高,我们的知识基础上有一个根本而巨大的漏洞。
与没有症状的人相比,有相当大比例的人患有一种名为Long-COVID的长期、经常使人虚弱的疾病。典型症状包括疲劳、呼吸困难、胸痛和心律失常。免疫学基础是可能的,但尚未确定。这些患者也没有接受系统的心血管评估,以确定可能的心肌炎或其他心脏异常,如纤维化,这可能是一些持久症状的原因。未来,如果患者出现不明原因的心肌病,并且SARS-CoV-2抗体检测呈阳性,这将不会令人惊讶。然而,考虑到感染的高流行率,将这种心肌病归因于病毒可能很困难,最终可能需要活检来确定病毒颗粒以支持因果关系。
运动员的心脏参与进一步提高了人们的担忧。一名从新冠肺炎康复的27岁职业篮球运动员在训练中猝死。俄亥俄州立大学(Ohio State University)的一项前瞻性研究发现,有几名大学生运动员患有心肌炎(14例),其中26例中有4例(15%),还有一名美国职业棒球大联盟的顶级投手。总体而言,这些年轻、健康的个体患有轻度新冠肺炎,但随后被发现患有意外的心脏病理。同样的人群-年轻人和健康人-在感染SARS-CoV-2后最常见的缺乏症状,这引发了有多少运动员患有隐匿性心脏病的问题。在了解更多之前,对SARS-CoV-2检测呈阳性的运动员进行系统评估,而不考虑症状,通过某种形式的心脏成像和心律失常筛查进行适当的控制似乎是谨慎的。
出现的最耐人寻味的问题是,为什么某些人在感染SARS-CoV-2后有心脏受累的倾向?一旦在大流行几个月后就认识到了这一点,人们的预期是心脏损害将主要发生在严重的新冠肺炎患者中。显然,它比预期的更常见,但真正的发病率尚不清楚。确定是什么导致了这一发病机制是至关重要的。它是否代表一个人的炎症反应,一种自身免疫现象,还是其他一些解释需要澄清。除了预防SARS-CoV-2感染之外,避免心血管受累的目标是最重要的。新冠肺炎的显著异质性,从缺乏症状到死亡,人们对此知之甚少。一种新出现的病毒在人类群体中广泛传播,具有各种各样的疾病表现,往往是神秘的,这使得解开这一点特别令人望而生畏。