SARS-CoV-2会成为地方病吗?
再感染是许多呼吸道病毒的一个显著特征,在这种情况下,一个人在一生中都会受到同一病毒种类的多种不同感染。事实上,常见的呼吸道病毒-包括流感病毒、呼吸道合胞病毒(RSV)、鼻病毒和地方性冠状病毒-在人类社会中的持续和普遍存在很大程度上是由于它们能够产生重复感染。自从导致正在进行的2019年冠状病毒病(新冠肺炎)大流行的严重急性呼吸综合征冠状病毒2型出现以来,一个关键的问题是人类是否会再次感染这种病原体,这可能使其成为地方病。
通常,在最初感染后,人类适应性免疫系统会形成一套防御系统,包括能够产生针对特定病原体的中和抗体的记忆B淋巴细胞,以及帮助调节免疫反应和诱导感染细胞死亡的记忆T淋巴细胞。这些适应性免疫成分,特别是B细胞,可以产生灭菌免疫,在这种免疫中,如果病原体再次进入宿主,就会阻止其在体内复制。
然而,对于许多病毒来说,许多过程,特别是获得性免疫反应不足、免疫力减弱和免疫逃逸,可以破坏或绕过免疫的杀菌特性,并允许随后的再次感染。在第一种情况下,最初感染特定病原体可能不会产生足以产生灭菌免疫力的获得性免疫反应。血清学研究表明,大多数SARS-CoV-2感染,无论严重程度如何,都会诱导某些特定抗体的产生(1);然而,尽管灵长类动物的实验性疫苗接种取得了令人鼓舞的结果,但这些抗体是否足以提供长期有效的保护,或者是否存在其他适应性免疫成分并发挥作用,仍不清楚。此外,对SARS-CoV-2感染的免疫反应是不同的,经历无症状感染的人表现出比经历更严重疾病的人更弱的免疫反应(1)。有可能一些个体在感染SARS-CoV-2后永远不会产生灭菌免疫,或者需要多次暴露才能亲和力成熟和形成持久的保护。
免疫力减弱,即最初的适应性免疫反应是强健的和保护性的,但随着时间的推移而消散,使宿主容易受到再次感染,也可能破坏灭菌免疫。免疫逃逸是第三个过程,可以促进再感染,特别是通过病毒感染。在这里,病毒在通过宿主群体连续连续传代的过程中,积累了点突变。这种聚集,称为抗原漂移,可能会导致病毒表面蛋白的构象变化,从而破坏先前产生的抗体与较早变异体的结合。免疫逃逸是这种抗原漂移的结果,这种漂移通过逃避适应性保护而使再次感染成为可能。
SARS-CoV-2免疫减弱和免疫逃逸的时间尺度因病原体不同而不同,尚未确定。到目前为止,SARS-CoV-2基因组的突变速度似乎比流感病毒慢。这种较低的比率可能是复制过程中校对的结果,这是RNA病毒中冠状病毒所独有的。相反,人类冠状病毒(HCoV)OC43是高度可变的,特别是在编码表面蛋白(如刺突蛋白)的基因上,表明可以发生相当大的多样性。到目前为止,在一项纵向研究中捕获了一些SARS-CoV-2特异性抗体减弱的证据(2),并记录了一些已证实的SARS-CoV-2重复感染(3)。虽然可能会发生再感染,但再感染病例的数量目前不足以概括人口规模的免疫持续时间或重复感染的严重程度。再感染是否会很常见,发生的频率如何,再感染的个人传染性如何,以及严重临床结果的风险是否会随着随后的感染而改变,仍有待了解。
从其他呼吸道病毒的洞察力表明,有可能再次感染SARS-CoV-2。对四种地方性HCoV(OC43、HKU1、229E和NL63)的自然获得性感染表明,在1年内再次感染相同的HCoV类型是常见的(4);连续感染相同的流感病毒株可能在不到2年内发生(5);还记录了成人在1年内再次感染RSV(6)。相比之下,更多对宿主产生全身影响的致病病毒可能会引发更持久的适应性免疫反应。例如,sars幸存者的纵向免疫图谱显示出更强的免疫应答。
地方性HCoV(OC43、HKU1、NL63和229E)在温带地区都表现出季节性,与流感病毒相似(12)。因此,许多研究试图确定温度、日照、湿度、臭氧和污染等条件是否会影响SARS-CoV-2的活性和传播性。目前的结果还不是决定性的,尽管似乎日照和湿度等环境条件可能会调节SARS-CoV-2的传播性-不足以阻止在免疫力普遍较低的大流行第一波期间传播-但一旦免疫力增强,可能足以支持冬季在温带地区进行季节性、锁相传播,类似于流感病毒。
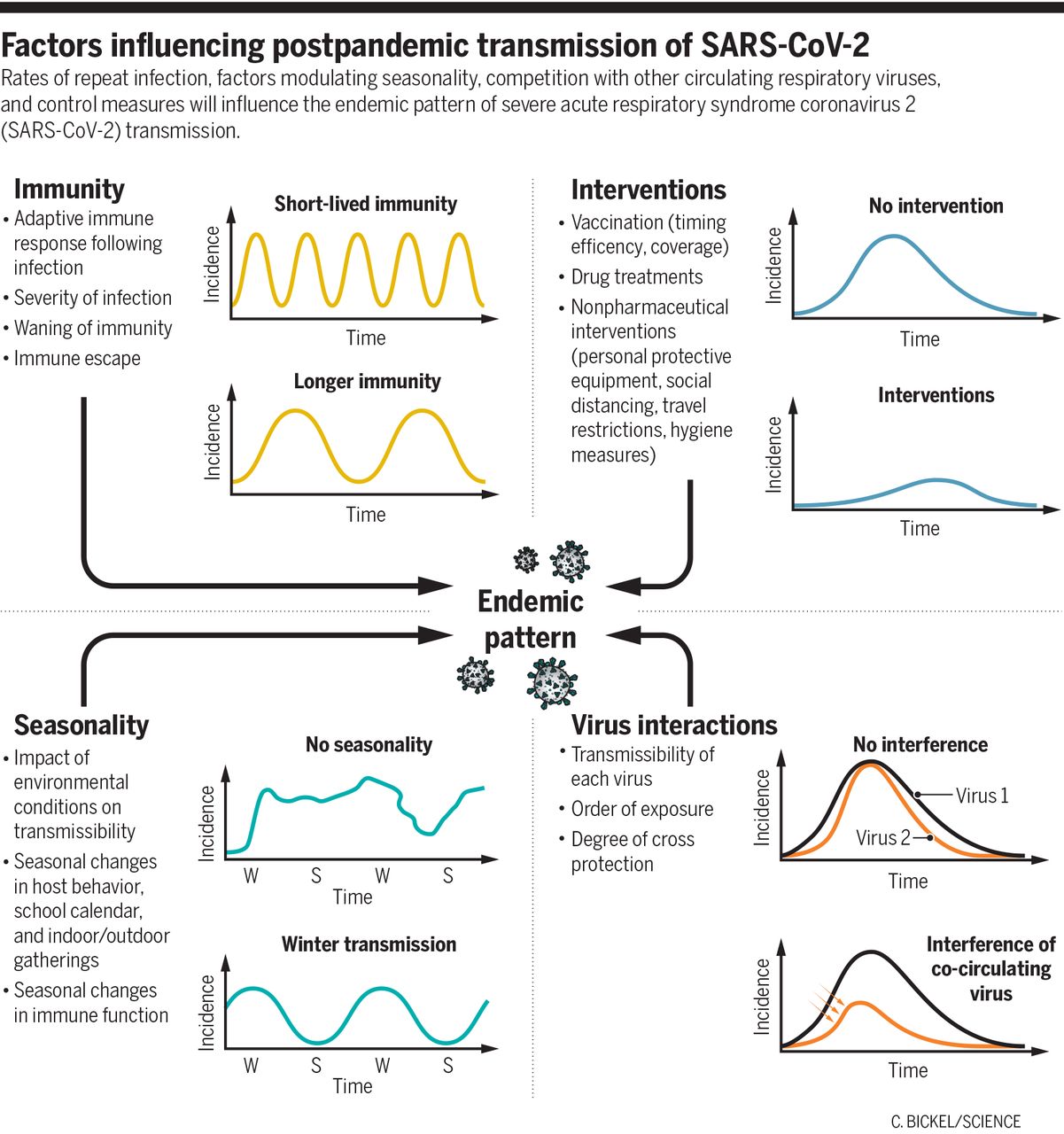
与2009年流感大流行一样,SARS-CoV-2在最初大流行期间之后的持续传播将表现为再感染率、疫苗可获得性和有效性以及调节病毒传播性的社会、免疫和先天因素的函数(见图)。此外,SARS-CoV-2在人类群体中的周期性持久性可能会受到与其他呼吸道病原体持续相互作用的机会的影响。
共同传播的呼吸道病毒在争夺相同资源的同时可能会相互干扰,它们之间的相互作用已经在群体和个体水平上、在重建的人体组织中和在动物模型中进行了研究。连续暴露于不同病毒的个体的结果各不相同,通常似乎取决于暴露的顺序和时间。许多研究都有证据表明,病毒之间的负面干扰是由第一次感染引起的短暂(天)保护引起的。宿主抗病毒干扰素反应通常被认为是干扰表现的主要机制,也就是说,由于最近的感染,宿主细胞上调干扰素的合成,潜在地抑制了二次感染。即使它是短暂的,但这种影响在人口规模上可能很强,并暂时降低病毒的流行率或改变其传播的时间。例如,假设2009年夏季鼻病毒大爆发推迟了欧洲大流行性流感病毒的出现(13)。
在未来几年,需要监测SARS-CoV-2与其他呼吸道病毒,特别是流感病毒和其他HCoV之间的临床和人群规模的相互作用。到目前为止,一些SARS-CoV-2混合感染已经被记录在案(14),包括与流感和RSV的联合感染;然而,对多种病原体的检测并不是例行的,而且确实存在的稀缺数据(主要是针对先前存在疾病的高比率的老年人)不支持对联合感染可能性或严重程度的明确评估。大流行前的研究表明,同时感染多种呼吸道病毒并不少见,但与疾病严重程度的增加无关。
在人口规模上,流感和SARS-CoV-2疫情之间可能存在重叠,对公共卫生系统构成严重威胁。季节性流感每年在全球产生数以百万计的严重感染,对于已经受到新冠肺炎大流行挑战的系统来说,这种额外的负担可能是灾难性的。相反,考虑到不同呼吸道病毒之间的传播方式相似,为减轻SARS-CoV-2传播而采取的非药物干预措施(个人防护装备、社交距离、提高卫生水平、限制室内聚会)可能会降低季节性流感爆发的程度。这种非药物措施的增加使用,以及可能的病毒干预,可能是最近南半球冬季流感发病率降低的原因(15)。
多病原体系统中不同爆发的阶段和程度由这些病原体之间的相互作用动力学决定:从病原体加强彼此传播时的大重叠阶段,到通过更具传播性的菌株的中和交叉反应来完全抑制一种菌株(9)。根据SARS-CoV-2与其他贝塔冠状病毒(OC43和HKU1)之间的免疫和交叉免疫的持续时间,已经对SARS-CoV-2的几种延迟流行情景进行了模拟(10),这取决于SARS-CoV-2与其他贝塔冠状病毒(OC43和HKU1)之间的免疫和交叉免疫的持续时间。与其他β冠状病毒相似的免疫持续时间(~40周)可能导致每年爆发SARS-CoV-2,而较长的免疫谱,加上对其他β冠状病毒的少量保护性交叉免疫,可能导致病毒明显消除,然后在几年后卷土重来。当然,其他情况也是可能的,因为有许多进程正在运行,而且很多过程仍未解决。
承认:J.S.和哥伦比亚大学拥有SK Analytics的部分股权。J.S.为BNI提供咨询服务。这项工作得到了美国国家航空航天局的支持