冠状病毒在细胞中形成触角的图像可能有助于识别治疗方法
与早先的指导方针不同,疾控中心现在表示,患有新冠肺炎的孕妇比未怀孕的妇女风险更高。今日美国。
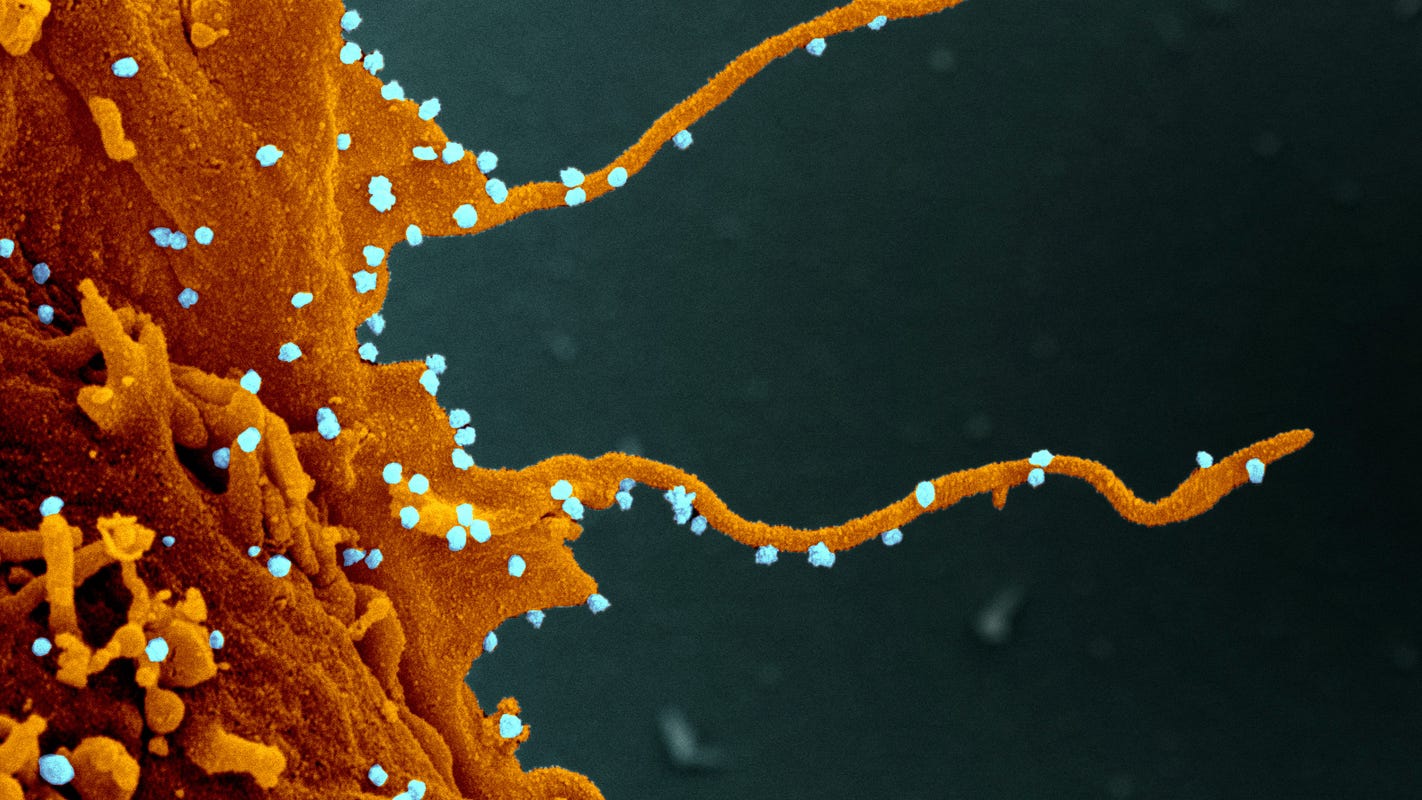
密尔沃基--令人震惊的、前所未见的图像显示,新的冠状病毒劫持了我们细胞中的蛋白质,形成了巨大的触角,这些触手会分叉开来,可能会将感染传播给邻近的细胞。
这一发现,以及一个国际科学家团队周六发表在《细胞》杂志上的证据,表明存在针对新冠肺炎的潜在更有效的药物。
取自结肠的人类上皮细胞,感染了导致新冠肺炎的SARS-CoV-2病毒的荧光显微镜图像。受感染的细胞产生触手,正式名称为丝状足(白色),从含有病毒颗粒(红色M蛋白)的细胞表面伸出。(图片来源:弗莱堡大学罗伯特·格罗斯博士)。
通过专注于病毒的基本行为-它如何劫持关键的人类蛋白质,并利用它们来造福于自己和伤害我们-该团队能够识别出一系列名为激酶抑制剂的现有药物,这些药物似乎为新冠肺炎提供了迄今最有效的治疗方法。
这篇新论文的70多名主要作者之一、加州大学旧金山分校(University of California,San Francisco)定量生物科学研究所(Quantity Biosciences Institute)所长内万·克罗根(Nevan Krogan)表示:我们已经测试了许多这样的激酶抑制剂,其中一些比瑞德韦尔更好。
虽然redesivir还没有被批准用于治疗新冠肺炎,但美国的监管机构已经允许大多数住院患者紧急使用该药。
Krogan说,对激酶抑制剂的测试显示,包括Gilteritnib和Ralimetinib在内的一些药物需要比雷米德韦更低的浓度,才能真正杀死50%的病毒。
这项新的研究涉及使用来自人类的细胞和其他来自非洲绿猴子的细胞进行实验,研究表明,这种被称为SARS-CoV-2的病毒特别擅长扰乱重要的通信。这些交流既可以在两个细胞内进行,也可以从一个细胞到另一个细胞进行。
一只感染了导致新冠肺炎的SARS-CoV-2病毒的雌性非洲绿猴肾脏细胞的电子显微镜图像。受感染的细胞产生正式名称为丝状足(橙色)的触须,从细胞表面伸出,使病毒颗粒(蓝色)发芽,并感染附近的细胞。(图片来源:NIAID/NIH伊丽莎白·费舍尔博士)。
这篇论文展示了病毒能够多么彻底地重新连接细胞内发生的所有信号。威斯康星大学麦迪逊分校(University of Wisconsin-Madison)医学微生物学和免疫学副教授安德鲁·梅尔(Andrew Mehle)表示,这真的很了不起,而且这种情况发生得非常快(最快在细胞感染后两个半小时)。
这个被称为细胞信令的通信系统允许细胞生长,并检测和应对外部威胁。细胞信号的错误可能会导致癌症和糖尿病等疾病。
Mehle没有参与这项研究,他说,这项工作表明,科学家们正在与一种新的冠状病毒中令人望而生畏的敌人作斗争。
他说,这些机器效率很高,经过进化调整,这将使开发治疗学变得非常具有挑战性。
从大流行的早期开始,Krogan和他的同事们采取了一种与许多寻求治疗这种新病毒的美国研究人员截然不同的方法。
许多科学家一直在对数以千计已经批准用于其他用途的药物进行筛选,以确定它们是否也可以用于治疗新冠肺炎。
克罗根说:我们不会这么做的。我们要说的是,让我们了解病毒如何感染我们背后的潜在生物学,并利用这一点来对抗病毒。
在寻找治疗方法的过程中,许多科学家专注于病毒中的关键蛋白质-特别是使病毒细胞能够附着在人类细胞上的刺突蛋白(Spike Protein)。
从结肠取来的人类上皮细胞的荧光显微镜图像,感染了导致新冠肺炎的SARS-CoV-2病毒。病毒N蛋白(红色)劫持人酪蛋白激酶II(绿色,黄色共存),推测产生分枝的丝状足突(白色轮廓框),使病毒颗粒发芽和感染附近的细胞。(图片来源:弗莱堡大学罗伯特·格罗斯博士)。
克罗根和他的团队朝相反的方向看,把重点放在人类蛋白质上,而不是病毒中的蛋白质上。数十种不同的人类蛋白在疾病过程中发挥着关键作用,因为病毒需要它们来感染人并复制自己。
开发针对人类蛋白质而不是病毒蛋白质的治疗方法有一个重要的优势。病毒蛋白可以发生变异,导致它们对针对它们的药物产生抗药性。人类蛋白质发生突变的可能性要小得多。
今年4月,Krogan和他的同事们在《自然》杂志上发表的一项研究显示,大约332种人类蛋白可以与27种病毒蛋白相互作用。
在克利夫兰临床基因组医学研究所经营实验室的博士研究员程飞雄(音译)称,这些蛋白质之间的相互作用图谱是一种新颖和强大的策略,可以找到可能有助于治疗新冠肺炎患者的现有药物。
在这项新的研究中,克罗根的国际团队对生物学进行了更深入的研究,重点研究了新型冠状病毒如何改变一个称为磷酸化的复杂过程。这一过程充当了不同细胞活动的一系列开关,包括细胞生长、分裂、死亡和相互沟通。
利哈伊大学(Lehigh University)生物科学教授林恩·卡西梅里斯(Lynne Cassimeris)表示,他们所做的一切真的是非常棒的下一步。他解释说,这项工作建立在前一篇论文的基础上,应用了过去30年来获得的细胞生物学知识。
这是一个惊人的飞跃。我们知道病毒一定是在操纵这些人类蛋白质。现在我们有了一张清单,上面列出了随着时间的推移正在发生的变化。
Cassimeris说,绘制这些变化的地图可以让研究人员寻找可以在特定时间点进行干预的药物。
科学家们发现,在与新型冠状病毒相互作用的332种蛋白质中,有40种蛋白质的开关发生了显著变化。
这些变化的发生是因为病毒可以向上或向下调节49种称为激酶的酶。激酶的向上或向下拨号导致它们改变了与病毒相互作用的40种蛋白质。
想象一下,激酶是保护我们健康的卫士,直到新的冠状病毒把它们变成对我们不利的。然而,在每种情况下,新的研究都确定了可以阻止病毒将警卫变成袭击者的治疗方法。
这种病毒最强大的劫持了一种名为CK2的激酶,它在细胞的基本框架结构以及细胞的生长、增殖和死亡过程中发挥着关键作用。
这导致科学家们对一种名为Silmitasertib的药物进行了研究。测试发现,这种药物可以抑制CK2基因,并消除这种新的冠状病毒。
一只感染了导致新冠肺炎的SARS-CoV-2病毒的非洲绿猴母猴肾脏细胞的电子显微镜图像。受感染的细胞产生正式名称为丝状足(橙色)的触须,从细胞表面伸出,使病毒颗粒(蓝色)发芽,并感染附近的细胞。(图片来源:NIAID/NIH伊丽莎白·费舍尔博士)。
他们还发现,该病毒对一条途径有戏剧性的影响-一组激酶形成的级联,有点像倒下的多米诺骨牌。病毒劫持了这种级联反应,所以最终结果变成了我们身体免疫系统的危险的过度反应。
这项研究在这条途径上的发现可能有助于解释极端的过度反应-一场严重的细胞因子风暴-导致免疫系统杀死健康和患病的组织,导致新冠肺炎一半以上的死亡。
在这里,科学家们也能够确定治疗方法,包括实验性抗癌药物雷米美替尼,它可能会防止免疫系统的过度反应。
这项新研究的作者还发现,该病毒损害了一种名为CDK的激酶家族。这些蛋白在细胞生长和对DNA损伤的反应中发挥作用。一种名为diaciclib的实验药物可能会有效地挫败这种病毒攻击。
最后,Krogan和他的同事们发现,该病毒还劫持了一种激酶,该激酶帮助细胞在不同环境中保持健康,并清除受损细胞,一种名为Apilimod的小分子以这种激酶为靶标,并已能够在实验室测试中阻碍病毒的传播。
克罗根也是加州大学旧金山分校格莱斯顿研究所(Gladstone Institutes)的研究员,他说,事实证明,检查受病毒影响的人类激酶的策略是卓有成效的。