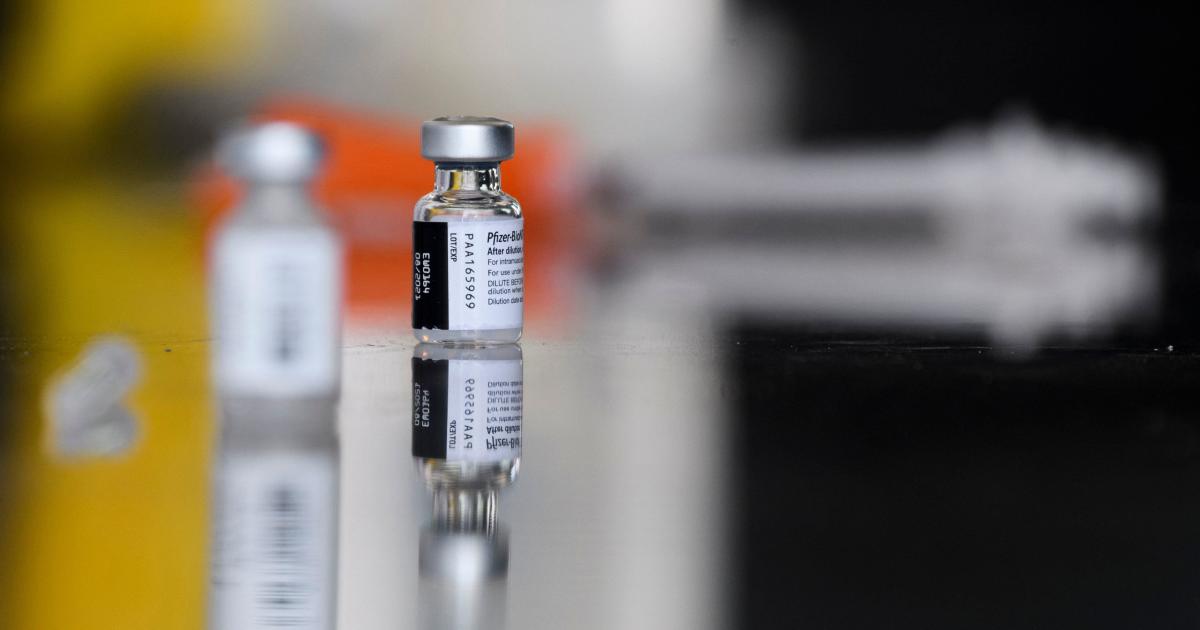
CDC计划Covid-19疫苗后稀有心脏炎症的“紧急会议”
疾病控制和预防的中心周四宣布它将召集AN"紧急会议"其顾问在6月18日讨论稀有但高于预期的心脏炎症后的报告,这些报告是基于mRNA的辉瑞和现代Covid-19疫苗。
到目前为止,CDC已经确定了226个可能会符合该机构' s"工作案例定义"拍摄后的心肌炎和心包炎,原子能机构周四透露。绝大多数已恢复,但41次持续症状,15次仍在住院,3个在重症监护室中。
该报告仅占近13亿美国人的小部分,这些美国人已经完全接种了辉瑞或现代的效果和#39;剂量。
"它的一点苹果到橘子比较,因为再次,这些是初步报告。并非所有这些都会成为真正的心肌炎或心膜炎报告,"警告CDC疫苗安全官员警告汤姆希姆瓦罗博士。
Shimabukuro表示,他们的发现大多是"一致"凭借在以色列研究的罕见心脏炎症病例报告,今年早些时候从美国国防部报道。
他说,CDC正在开展更多数据和分析下周在其自身顾问的紧急会议之前的报告,并计划分析捕获Covid-19带来的心脏炎症的风险。
有关心肌炎和心包炎的新细节首先出现了一个关于粮食和药物管理局的独立顾问小组的介绍,他周四会议讨论监管机构如何接近您在年幼儿童中使用Covid-19疫苗的紧急使用授权。
在上个月享受股份有限公司的美国Covid-19疫苗的紧急用途授权后,辉瑞公司本周宣布,它已经决定在儿童临床试验中使用,以6个月大为6个月,并希望提交数据十月。 Modgea周四表示,它也要求FDA'允许将其mRNA疫苗与青少年寄予。
虽然辉瑞表示,他们希望在9月份将儿童的审判包装为2月2日,FDA官员曾提醒过该年龄群体的授权疫苗可能需要更长时间 - "中期秋季下降秋季;最早 - 引用他们收到镜头后为儿童所需的额外后续数据。
"我们认识到,今天早些时候讨论的某些不良反应,例如心动炎或心膜膜炎,可能太不常见,无法检测在许可前临床试验的典型大小的安全数据库中," Doran Fink博士说,FDA' S疫苗办公室的顶级官员。
疾病预防控制中心此前透露,主要是在跟随他们的第二剂年轻男子和少年检测心脏炎的报告,并认为有"较多的观察到比预期" 16到24岁的案件。上个月,CDC敦促提供商"询问先前的Covid-19疫苗接种"在患有心脏炎症症状的患者中。
"确定是否发布用于使用Covid-19疫苗的紧急使用授权进入健康的儿科个人的风险效益的考虑将需要考虑这些信息,并且风险效益考虑可能是不同的,而不仅仅是相比对于成年人而言,他们也可能对年轻的比较年龄较大的儿科群体不同,而且他们也可能是不同的。 FDA'疫苗办公室主任Marion Gruber博士在会议上表示。