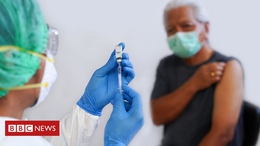
首批COVID-19疫苗今天已向FDA申请紧急授权
今天,美国食品药品监督管理局将首次提交候选疫苗来对抗大流行性冠状病毒。
制药巨头辉瑞公司和德国生物技术公司BioNTech今天凌晨宣布,他们正在提交正式请求,要求从FDA获得该公司的mRNA疫苗BNT162b2的紧急使用授权(EUA)。
提交该文件之前,就在周三的著名新闻中,两家公司已经结束了其III期临床试验,发现该疫苗在预防有症状的COVID-19(冠状病毒SARS-CoV-2引起的疾病)方面具有95%的有效率。
尽管尚未公布有关该试验的全部数据,但两家公司在新闻稿中宣布,该疫苗在种族和族裔背景下似乎一直有效,对65岁以上的人群(严重疾病风险最高的年龄段)的患者有效率为94%。试验数据还表明,该疫苗可预防严重疾病和轻度病例。
该试验达到终点时,共有43661名参与者参加了170例病例,这些参与者来自美国,德国,土耳其,南非,巴西和阿根廷的150个试验地点之一。在170例病例中,安慰剂组为162例,接受实验性两剂疫苗的组中只有8例发生了。在所有病例中,有10例严重,其中9例属于安慰剂组。
除了令人印象深刻的功效数字外,两家公司还将向FDA提交有关8,000名随机选择的成人参与者的详细安全报告,以及大约38,000名在第二剂疫苗接种后两个月中位数受到被动监测的成人参与者的数据。此外,这些公司还提供了100名12至15岁儿童的安全性数据。这些公司报告称,对该疫苗没有严重反应,最令人讨厌的副作用包括严重的头痛和疲劳。
目前尚不清楚FDA需要多长时间来审核EUA要求。但是,FDA一再表示将致力于迅速采取行动,以应对可怕的健康危机,而这一危机在日益恶化。
我们提供安全有效的疫苗的工作从未像现在这样紧迫,因为我们继续看到全球COVID-19病例数量惊人地增加。在美国归档代表了我们向世界提供COVID-19疫苗的过程中的关键里程碑,我们现在对疫苗的功效和安全性有了更全面的了解,这使我们对其疫苗的潜力充满信心。
两家公司表示,他们也正在准备向全球其他监管机构提交材料,包括向欧洲药品管理局提交的材料。
他们在公告中表示,辉瑞和BioNTech“将准备在授权后数小时内分发候选疫苗。”
两人的制造能力到2020年全球将生产多达5000万剂疫苗,到2021年底将达到13亿剂疫苗。两家公司已与美国政府达成协议,将提供1亿剂疫苗,足以为5000万人接种疫苗。 -美国可以选择再购买5亿美元。