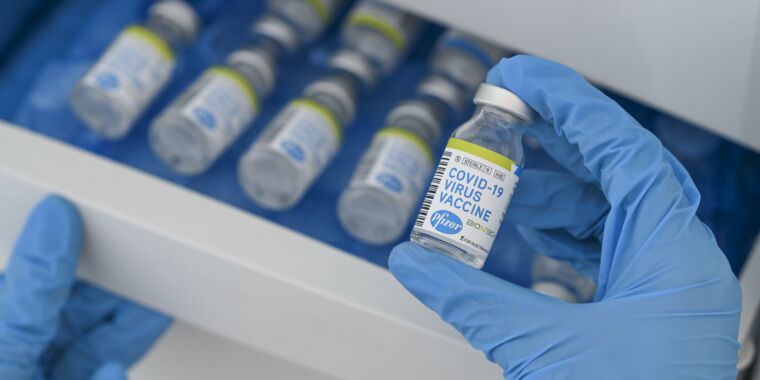
据报道,FDA计划在几天内授权青少年12-15的辉瑞的Covid疫苗
根据纽约时报的报告,食品和药物管理局计划授权在青少年或下周晚些时候的青少年中使用PFizer-Biontech的Covid-19疫苗。
时代引用未命名的联邦官员,这些联邦官员没有授权公开发言FDA计划。如果FDA在本周授权使用青少年组中的疫苗,则疾病控制和预防的疫苗咨询小组的中心将可能一天举行审查临床试验数据并提出一项关于使用的推荐,次数报告。
3月31日,辉瑞公司宣布,疫苗在一小期III期临床试验中,疫苗在12至15岁的青少年反对Covid-19。疫苗在年龄组中也良好耐受,主要生产标准副作用。
在2,260人的试验中,1,131名青少年12至15岁接受疫苗,而1,129则获得安慰剂。试验中有18例症状Covid-19,所有这些都在安慰剂组中。辉瑞指出,疫苗接种组似乎在较早的水平下产生的中和抗体,辉稿器指出。
“我们分享了扩大疫苗授权的紧迫感,以利用年龄较小的人群,并通过12和15岁的青少年的临床试验数据鼓励,”辉瑞公司的首席执行官Albert Bourla之间的青少年之间的临床试验数据。 “我们计划将这些数据提交到FDA,作为对未来几周的紧急使用授权以及世界各地的其他监管机构的拟议修正案,希望在下一学年开始之前将该年龄组接种疫苗。”
辉瑞和比翁科技正在致力于6个月至2年,2至5岁的儿童临床试验和5至11年。 PFizer-Biontech疫苗目前仅授权用于16岁及以上的人。
到目前为止,美国超过1.05亿人口 - 约有32%的人口 - 已完全针对Covid-19接种疫苗。超过1.47亿 - 约44% - 至少有一剂。但美国疫苗接种率为4月中旬以来,每天230万左右,每天下降约260万疫苗接种。在青少年使用PFizer-Biontech疫苗的授权可以在夏季活动之前再次对该国的疫苗进行繁殖需求,并在秋季开始上学。
我喜欢看到这些决策过程的最终的潜水,看看ARS更深入。 FDA似乎绝对可能有它需要做到这一点的需求。什么是防止他们在吃火腿三明治之后的那个公告?这是' t"只是询问问题*"或者其他 - 我和#39;米合法好奇。现在和下周早期或下周早期会发生什么变化?收集哪些信息,以进一步通知此过程?
按顺序获取所有文档并审核,确保在提交之前一切顺利。
该过程包括让专家建议加上公众的建议。所有FDA咨询委员会会议都在流动,并在线提供。这是一天中更好的部分,但是通过听力,甚至是旧的,是非常富有作用的。该过程允许多个观点和讨论。投票没有约束力:FDA可以遵循投票或不遵循并可以遵循这些建议。但是,该过程意味着每一个都看到相同的数据并表达他们的观点o意思。实际上,来自&#34的数据;赞助商"并在几天前在线提供单独的FDA分析。好奇地,一些州非常关注,这一进程不够彻底,因为他们在允许其国家使用的疫苗之前决定有自己的审查。随后的评论成为Pro Forma Rubber Stamps,一旦他们看到FDA的小心。花一些时间来看看旧会议或在审查数据后拍摄此类会议。以下是与janssen疫苗的FDA讨论的链接:https://www.fda.gov / adadis-committees ......这里是全新8小时会议的链接(包括所有休息):https:/ /www.youtube.com/watch?v=qd7mlcd-rea在这里是即将到来的所有咨询委员会的会议:https://www.fda.gov / adadisory-committees ...电子日历请本周查看日历,查看疫苗委员会的任何即将到来的会议。日历最后于4月29日上次更新(截至2010年5月4日,截至2011年5月4日)。